

乳癌
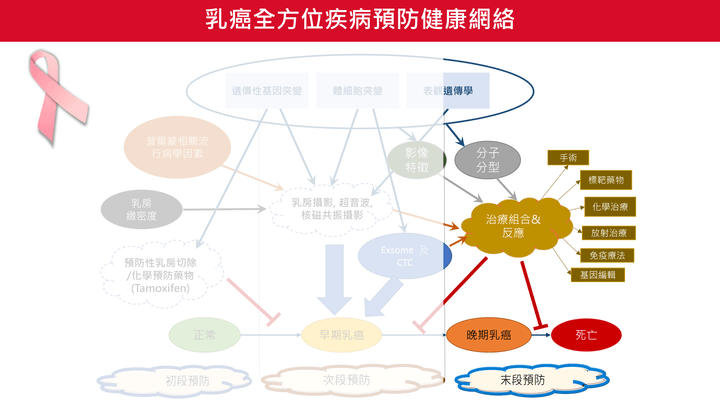
乳癌全方位疾病預防健康網絡:治療與末段預防
乳癌防治不僅止於健康促進與篩檢,更需要跨專業整合的治療策略,以降低晚期乳癌致死率。
- 多模態評估後導入治療決策
- 透過影像特徵、液態活檢(Exosome、CTC)、分子分型等資訊整合,針對不同乳癌亞型制定個別化治療計畫。
- 主要治療模式包含
- 手術治療:切除病灶、乳房重建。
- 化學治療:依據腫瘤分期與基因表現選擇藥物。
- 放射治療:局部控制、降低復發。
- 標靶藥物:針對HER2、PI3K、CDK4/6等分子作用靶點。
- 免疫療法:提升體內免疫系統對癌細胞的辨識與清除能力。
- 基因編輯(如CRISPR):新興策略,未來可能用於調控腫瘤生長機制。
- 治療反應監測與調整,持續追蹤治療效果,動態調整方案。整合AI與數據預測模型,提升預後判斷精確度。
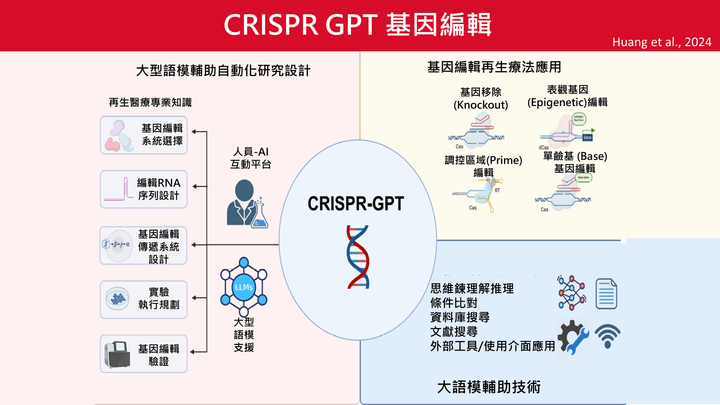
CRISPR GPT 基因編輯
- 利用大型語言模型(GPT)整合生物資訊與實驗設計,可自動化協助基因編輯研究流程。
- 應用AI生成式模型進行RNA序列設計、目標基因選擇、引導RNA(gRNA)合成與優化,提高效率與準確性。
- CRISPR-GPT平台結合知識圖譜與深度學習,有助於推進複雜疾病相關基因的識別與功能預測。
- 支援多種基因編輯模式,包括基因敲除(Knockout)、基因調控(Epigenetic)、精準編輯(Prime/Base Editing)。此技術不僅提升編輯效率,也降低脫靶率,為乳癌等重大疾病的基因療法奠定基礎。
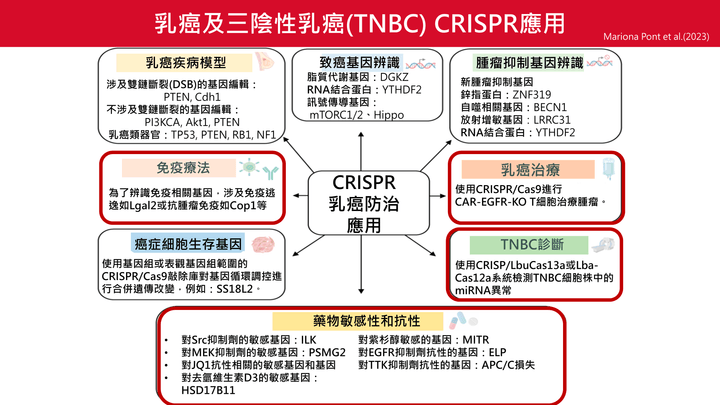
乳癌及三陰性乳癌(TNBC)CRISPR應用
- CRISPR基因編輯技術廣泛應用於乳癌治療策略,包括腫瘤免疫逃脫機轉解析、藥物靶點確認及轉移抑制。
- 在乳癌免疫療法中,透過調控PD1/PD-L1路徑與免疫檢查點(如CD44)可增強T細胞活性與腫瘤抑制效果。
- 三陰性乳癌(TNBC)因缺乏ER/PR/Her2受體,治療困難,CRISPR可用於導入標靶基因(如BRCA1/2)或微RNA通路,以改善預後。
- 在癌細胞生存與轉移方面,可靶向調節轉移相關基因(如S100A4)、代謝通路(如YTHDF2)與上皮間質轉換(EMT)路徑。
- CRISPR亦可用於藥物敏感性提升與個人化醫療,例如針對ILK、HSP90、APC等特定標的進行功能性基因編輯。
大腸癌
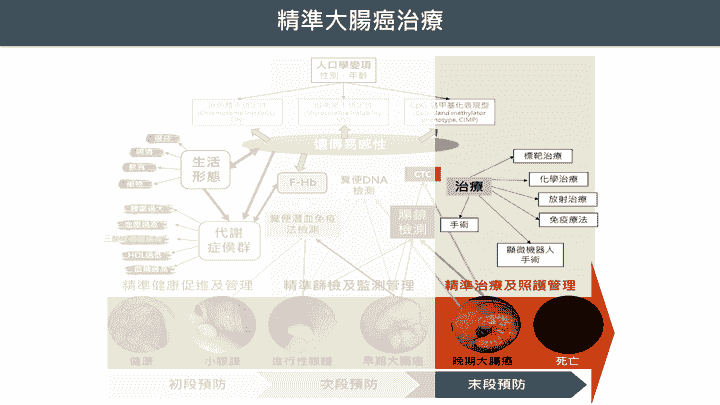
精準大腸癌治療
- 在大腸癌的「末段預防」階段,進入疾病後期後,強調的是精準治療與照護管理。依據腫瘤的分子特徵(如微衛星不穩定性、染色體不穩定性、CpG島甲基化表現型等)進行個人化分型治療,包括標靶治療、化學治療、免疫治療與放射治療等多元策略,並可輔以微創與機器人手術技術,提高治療精準度與生活品質。
慢性病
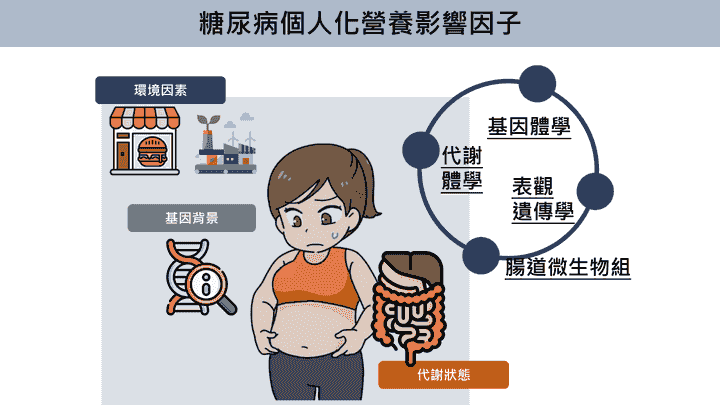
糖尿病個人化營養影響因子
- 糖尿病罹病風險受到包含環境因素(如飲食習慣與生活型態)、個人的基因背景與代謝狀態,以及腸道微生物組的組成、基因體學、代謝體學、表觀遺傳學等多元、多層次、多重因素交互影響。這些因素共同決定每個人對營養與治療的反應。疾病控制效果與生活品質需仰賴個人化糖尿病營養策略。

個人化最佳營養建議-飲食重要性
- 特定飲食型態如地中海飲食、高纖維與低GI食物有助於血糖控制。飲食也會與運動和降血糖藥物產生交互影響。糖尿病與飲食營養建議須個人化並整合運動與用藥考量。
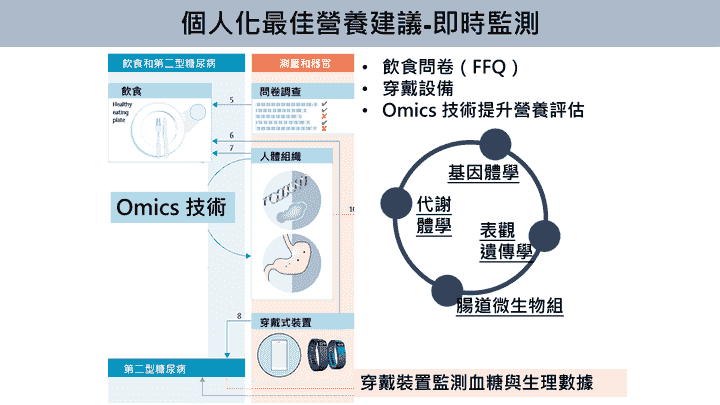
個人化最佳營養建議-即時監測
- 透過大型語言模型飲食問卷、基因體學、代謝體學、腸道微生物等Omics 技術結合穿戴設備可即時追蹤血糖與生理數據,提供飲食介入血糖反應即時回饋,精確評估營養狀態與介入相關代謝反應,有助於糖尿病個案個人化飲食建議與營養管理。
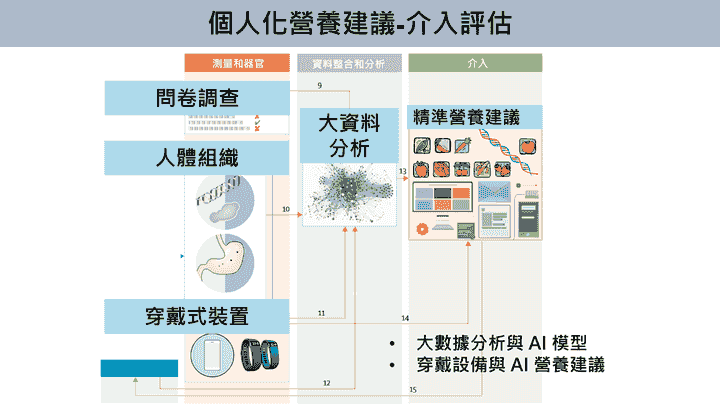
個人化營養建議-介入評估
- 透過大型語言模型問卷、生化檢測與穿戴式裝置蒐集資料,經由大數據分析與AI模型整合,利用大型語言模型提供精準營養建議,提供更符合個人需求的飲食營養介入策略,提高糖尿病管理成效。
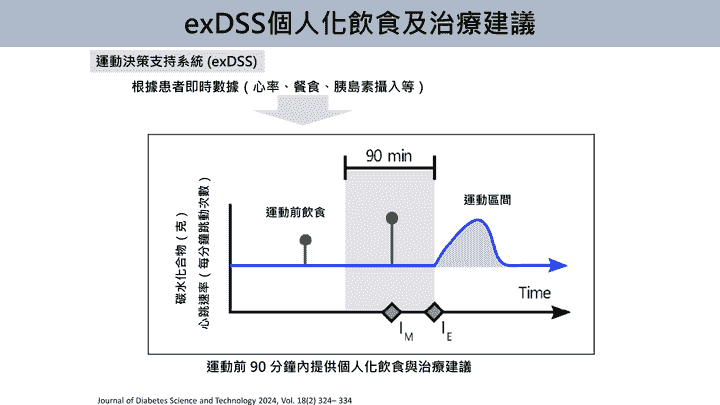
exDSS個人化飲食及治療建議
- 運動決策支持系統(exercise Decision Support System, exDSS)根據患者即時數據(如心率、飲食、胰島素攝入等),在運動前90分鐘內提供個人化的飲食與治療建議。運用個人化智慧決策系統可在運動前建議適量攝取碳水化合物,穩定運動期間的血糖與能量供應,提高運動安全與效果。
第二型糖尿病個人化幹細胞治療應用實例
- 患者為59歲男性,罹病25年併發末期糖尿病腎病變,已於2017年接受腎臟移植。由於血糖控制不穩、波動劇烈(MAGE達100 mg/dL),高低血糖事件頻繁,影響腎臟植體存活,患者於2019年底接受自體幹細胞胰島移植療法。
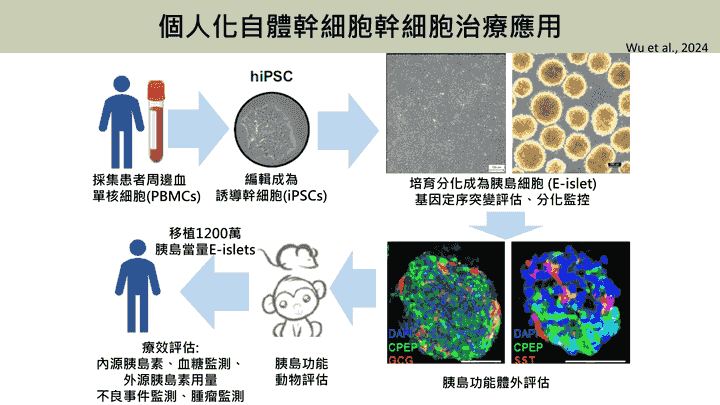
個人化自體幹細胞幹細胞治療應用
- 個人化幹細胞治療首先收集病患周邊血單核細胞(PBMCs),經重編程成誘導性多能幹細胞(iPSCs),培育並分化成胰島細胞(E-islets),過程中進行基因定序與分化監控。後續將1,200萬顆胰島細胞移植回患者體內,並透過體外與動物實驗評估所收集幹細胞功能與安全性。幹細胞移植療法後續監測包括血糖監測、內外源性胰島素用量監測、不良事件與腫瘤風險評估等。
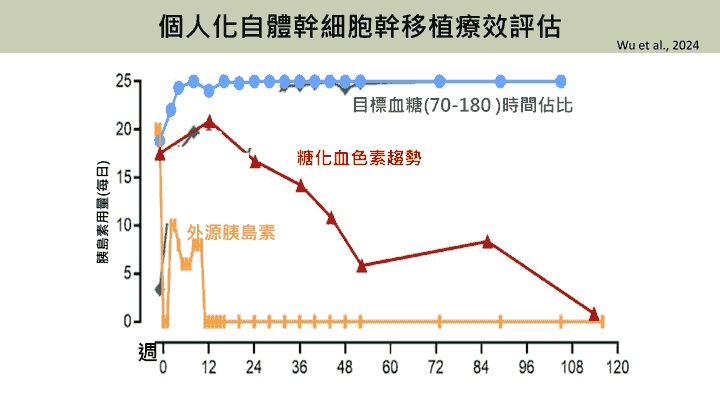
個人化自體幹細胞幹移植療效評估
- 治療後第2週起,患者血糖控制顯著改善,目標血糖時間佔比提高至78%,高血糖與低血糖事件消失,且內源性胰島素分泌明顯增加。第11週成功停用外源胰島素,第56週停用口服藥。至第116週追蹤期間未發生低血糖或腫瘤問題。不良事件輕微包括短期腹脹、食慾減低與輕微體重減輕(80公斤降至76公斤),顯示幹細胞移植療法之穩定效果。
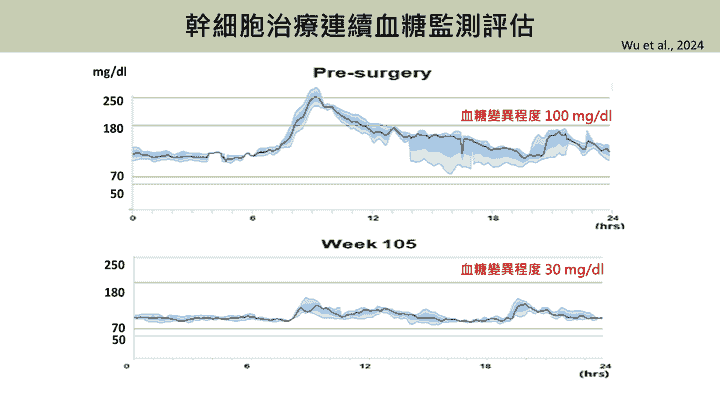
幹細胞治療連續血糖監測評估
- 手術前(Pre-surgery)病患血糖波動幅度大,連續血糖監測(CGM) 變異程度達100 mg/dL,常超出正常變異範圍。而在治療105週後(Week 105),血糖趨勢穩定變異度縮小至 30 mg/dL,顯示幹細胞療法對血糖穩定控制效益。
Copyright © 2019 - Strikingly 提供技術支援













